I geni sono alla base degli effetti cerebrali della leucemia
Alcuni bambini trattati per la leucemia linfoblastica acuta (LLA) sviluppano disturbi cerebrali e il rischio che ciò accada può essere collegato a determinati geni.
ALL è il cancro più comune durante l'infanzia e circa il 90% dei pazienti sopravvive. Ma il trattamento, che di solito include la chemioterapia e può includere radiazioni craniche, può innescare problemi a lungo termine con la memoria, l'apprendimento o altre funzioni cognitive.
La compromissione della memoria è un sintomo particolarmente debilitante, a causa del ruolo centrale che la memoria gioca nella vita quotidiana e nel successo scolastico o lavorativo.
Ora, Deborah Waber, Ph.D e colleghi del Boston Children’s Hospital, Massachusetts, Stati Uniti, hanno trovato quattro varianti genetiche specifiche che sembrano aumentare il rischio. Queste varianti sono correlate all'infiammazione del cervello e alla risposta delle cellule ai danni da stress ossidativo, come il danno cellulare causato dalla chemioterapia.
Hanno fatto la scoperta utilizzando campioni di sangue conservati e risultati dei test di funzione cognitiva su 350 TUTTI i sopravvissuti dagli Stati Uniti e dal Canada. I test cognitivi includevano comportamenti di QI, memoria, capacità di attenzione e iperattività.
I quattro geni evidenziati, NOS3, SLCO2A1, HFE e COMT, facevano parte di un gruppo di 28 geni studiati a causa del loro ruolo nel metabolismo dei farmaci o nelle risposte al danno cellulare.
Varianti specifiche di questi quattro erano "significativamente associate a effetti neurocognitivi", riferisce il team. Tutti sono coinvolti nei percorsi che regolano l'infiammazione nel cervello o proteggono le cellule dallo stress ossidativo.
Waber ha affermato: “Il nostro obiettivo è essere in grado di identificare chi è a rischio di effetti cognitivi tardivi e fornire interventi neuroprotettivi. Questa analisi retrospettiva ci dice che andando avanti potremmo voler esaminare i genotipi dei bambini al basale e condurre ricerche prospettiche per capire perché queste specifiche varianti genetiche possono aumentare il rischio di tossicità ".
I risultati dello studio sono stati presentati alla 56a riunione annuale dell'American Society of Hematology, tenutasi a dicembre 2014. Il team spera che sarà possibile eseguire lo screening genomico di TUTTI i pazienti per il rischio di memoria a lungo termine, attenzione e effetti di apprendimento.
L'autore principale, Peter Cole, M.D., ha dichiarato: “Più guardiamo, più scopriamo che molti sopravvissuti sperimentano cambiamenti nel modo in cui pensano. Se diamo a TUTTI i pazienti lo stesso trattamento, perché alcuni di loro hanno deficit di memoria o cognitivi, ma non tutti?
"Ci siamo limitati a varianti che sono presenti in almeno il 10 per cento della popolazione, decidendo che eravamo interessati a spiegare cosa potrebbe accadere nella maggior parte dei pazienti".
Nonostante i risultati significativi, Cole aggiunge che è necessario lavorare ulteriormente per confermare il ruolo dei quattro geni. Uno studio prospettico, in cui i geni dei pazienti vengono testati prima del trattamento, fornirebbe prove più affidabili.
Inoltre, qualsiasi intervento di protezione deve essere sottoposto a test preclinici e clinici per garantire che il successo del trattamento non sia compromesso.
Il co-autore Lewis Silverman, M.D., ha affermato: “Una delle principali priorità in corso nell'infanzia TUTTA la ricerca clinica è ridurre la tossicità del trattamento e certamente vogliamo ridurre gli effetti neurocognitivi tardivi, se possibile.
"Si spera che questo lavoro porti a un modo per identificare quei pazienti a più alto rischio di effetti tardivi neurocognitivi in cui possiamo concentrare i nostri sforzi di ricerca, aggiustando il nostro approccio terapeutico o testando nuove strategie protettive con l'obiettivo di ridurre gli effetti senza influire negativamente sulla possibilità per la cura. "
Waber ha aggiunto che il suo lavoro sull'impatto cerebrale di TUTTI i trattamenti abbraccia dieci istituzioni che collaborano in Nord America. I suoi primi studi hanno evidenziato un impatto cognitivo significativo tra i bambini trattati con successo per ALL, e hanno mostrato "una drammatica differenza di sesso, con le femmine molto più vulnerabili alla tossicità".
Gli oncologi pediatrici hanno cercato a lungo terapie meno tossiche. "La riduzione della dose o l'eliminazione delle radiazioni craniche ha portato a un miglioramento significativo dei risultati cognitivi, in particolare per le donne", ha detto Waber.
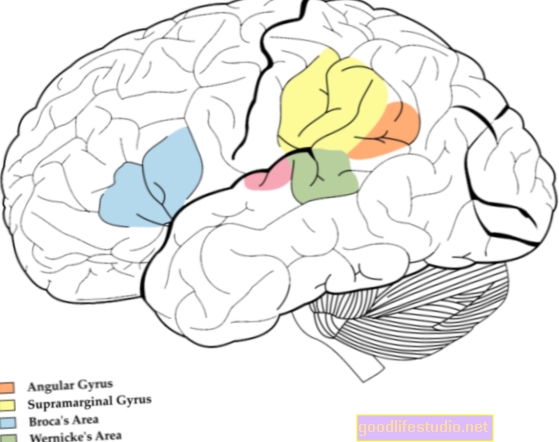
Il lavoro attuale si concentra sulle particolari aree del cervello che mostrano i danni maggiori. Waber ha detto: "L'ippocampo è fondamentale per la codifica della memoria episodica ed è squisitamente vulnerabile alla chemioterapia e alla radioterapia".
Deficit nella codifica e nell'apprendimento della memoria, nella memoria di lavoro, nell'attenzione, nella velocità di elaborazione delle informazioni e nelle abilità visuospaziali "si localizzano neuroanatomicamente nell'ippocampo nei lobi temporali mediali e nei lobi frontali".
Le radiazioni e la chemioterapia danneggiano le cellule staminali neurali dell'ippocampo e le cellule precursori, ostacolando il loro rinnovamento e trattenendo la mielinizzazione, il processo vitale in cui le cellule cerebrali sviluppano una guaina isolante che accelera i segnali cerebrali, non completamente completa fino all'età di circa 30 anni. Questi cambiamenti sono stati osservati nell'autopsia di individui trattati per tumori cerebrali primari e leucemia.
"Presi insieme", ha concluso Waber, "questi risultati forniscono una base funzionale e strutturale per alcuni dei sintomi cognitivi sperimentati dai sopravvissuti alla leucemia infantile".
Riferimento
Trial riferito al 56 ° meeting annuale dell'American Society of Hematology annual meeting, tenutosi dal 6 al 9 dicembre 2014, presso il Moscone Center, San Francisco, CA.